Diffusie
Iedere stof heeft de neiging zichzelf evenredig te verspreiden over de beschikbare ruimte (thee verspreidt zich door een glas heet water, geur verspreidt zich over de hele ruimte, etc). Dit heet diffusie (zie afbeelding).
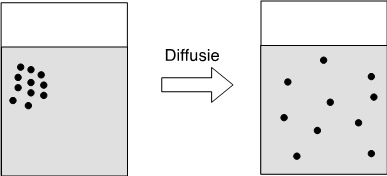
Als de concentratie van een bepaalde stof, bijvoorbeeld zuurstof, buiten de cel hoger is dan in de cel, zal de zuurstof van de plaats met hoge concentratie zich verplaatsen naar de plaats met de laagste concentratie, tot de concentratie aan beide zijden gelijk is. Dit gebeurt bijvoorbeeld in de longen bij ademhaling, waarbij zuurstof vanuit de longen naar het zuurstofarme bloed diffundeert.
De celmembraan scheidt stoffen buiten en binnen de cel van elkaar. Kleine moleculen, zoals zuurstof en koolstofdioxide, kunnen echter wel door deze membraan heen diffunderen. Andere stoffen, zoals glucose en geladen ionen zoals natrium-, kalium- en chloride-ionen, kunnen alleen door de celmembraan verplaatsen als er een transporteiwit aanwezig is dat een kanaal door de membraan vormt waar deze stoffen doorheen kunnen. Verplaatsing gaat dan altijd naar de plaats met de laagste concentratie. Deze vorm van transport kost geen energie en heet daarom passief transport.
Osmose
Ook water kan door passief transport verplaatsen naar de plaats met de laagste concentratie waterdeeltjes (dus met de hoogste concentratie opgeloste stoffen). Diffusie van water heet ook wel osmose.
Veel processen in het lichaam worden mogelijk gemaakt door osmose: zo nemen we vocht in het bloed op door osmose en scheiden we vocht uit via urine door osmose. Het is dan ook belangrijk dat de concentratie opgeloste stoffen in het bloed redelijk constant is. Is dat niet het geval, dan kan vochtophoping in de weefsels ontstaan (oedeem).
Osmose is ook in planten een belangrijk proces. De vacuolen in planten bevatten relatief veel opgeloste stoffen. Daardoor nemen plantencellen water op in hun vacuolen. De vacuole zwelt op, en de hele cel wordt groter, totdat de celmembraan tegen de celwand drukt. Hierdoor worden de planten stevig; de steel strekt zich uit. Zo kunnen kruidplanten rechtop staan.
Een zout milieu is voor cellen dan ook een probleem; de hoge concentratie zouten opgelost in de omgeving onttrekt vocht aan de cellen (denk aan zout op slakken). Alleen organismen die daarop zijn aangepast en bijvoorbeeld water actief naar buiten kunnen pompen, kunnen een zout milieu overleven.
Voor osmose zijn de volgende begrippen belangrijk:
- Osmostische waarde: hoe hoger de osmostische waarde, hoe hoger de hoeveelheid opgeloste stoffen ten opzichte van de omgeving, dus hoe meer water naar die plaats toe zal gaan.
- Isotoon: dezelfde osmotische waarde als de omgeving. Er vindt dus geen nettoverplaatsing van water plaats.
- Hypertoon: een hoge osmotische waarde. Een cel in een hypertone oplossing zal water afgeven aan zijn omgeving. De cel krimpt hierdoor (let op: er kan ook gesproken worden over een hypertone ccel; in dat geval is de osmotische waarde in de cel juist hoog en zal de cel water uit de omgeving opnemen).
- Hypotoon: een lage osmostische waarde ten opzichte van de omgeving. Een cel in een hypotone oplossing zal water opnemen. Heeft de cel geen celwand (dierlijke cel), dan zal de cel uiteindelijk “ontploffen”. Een hypotone cel zal juist water aan de omgeving afgeven, omdat in dat geval de osmotische waarde van de omgeving juist hoger is dan de osmotische waarde in de cel. Lees de informatie bij een vraag dus nauwkeurig!

