Als de coëfficiënten in een reactievergelijking niet gegeven zijn, kan men die als volgt bepalen:
- Kies een atoomsoort die aan beide kanten van de vergelijking in maar één formule voorkomt. Breng deze atoomsoort in evenwicht door coëfficiënten te kiezen. Schrijf deze coëfficiënten in de vergelijking, zelfs als deze gelijk zijn aan “1”.
- Kies een andere atoomsoort waarvoor alle coëfficiënten op één na bekend zijn. Bepaal de missende coëfficiënt.
- Als er breuken ontstaan, vermenigvuldig alle coëfficiënten met de gemeenschappelijke noemer.
- Herhaal deze stappen voor alle atoomsoorten in de vergelijking.
Let op: Bij het in evenwicht brengen van een vergelijking mag men de formules van stoffen niet veranderen. Zo kan men niet zomaar H2O door H3O vervangen.
Breng in evenwicht: $\mathrm{Fe + O_2 \to Fe_2O_3}.$
Zowel Fe en O komen aan beide kanten in maar één formule voor. Het maakt dus niet heel veel uit waar we beginnen. Laten we beginnen met Fe.
$$\mathrm{2 Fe + \text{__}\ O_2 \to 1\ Fe_2O_3}.$$
Nu bekijken we O. Rechts staan er drie O-atomen, dus moeten we er links ook drie hebben:
$$\mathrm{2\ Fe + \mathbf{1\frac12}\ O_2 \to 1\ Fe_2O_3}.$$
Om van de breuk kwijt te raken, vermenigvuldigen we alles met twee.
$$\mathrm{4\ Fe + 3\ O_2 \to 2\ Fe_2O_3}.$$
Breng in evenwicht: $\mathrm{Al + NH_4ClO_4 \to Al_2O_3 + AlCl_3 + N_2 + H_2O}$.
De atoomsoorten Al en O komen meer dan eens voor aan de rechterkant; begin daar dus niet mee. Ik kies ervoor om met N te beginnen:
$$\mathrm{\text{__}\ Al + \mathbf{2}\ NH_4ClO_4 \to \text{__}\ Al_2O_3 + \text{__}\ AlCl_3 + \mathbf{1}\ N_2 + \text{__}\ H_2O}.$$
Voor Cl is er nu maar één onbekende coëfficiënt. Breng de twee Cl-atomen links in evenwicht met AlCl3:
$$\mathrm{\text{__}\ Al + 2\ NH_4ClO_4 \to \text{__}\ Al_2O_3 + \mathbf{\frac 2 3}\ AlCl_3 + 1\ N_2 + \text{__}\ H_2O}.$$
Breuken wegwerken door met 3 te vermenigvuldigen:
$$\mathrm{\text{__}\ Al + 6\ NH_4ClO_4 \to \text{__}\ Al_2O_3 + 2\ AlCl_3 + 3\ N_2 + \text{__}\ H_2O}.$$
Voor H is er één onbekende coëfficiënt. Links staan er 24 H-atomen; daarom:
$$\mathrm{\text{__}\ Al + 6\ NH_4ClO_4 \to \text{__}\ Al_2O_3 + 2\ AlCl_3 + 3\ N_2 + \mathbf{12}\ H_2O}.$$
Voor O is er nog maar één onbekende coëfficiënt over. Links hebben we 24 O-atomen; rechts zijn er 12 O-atomen in H2O, dus moeten de overige 12 bij de Al2O3 vandaan komen. Zodoende:
$$\mathrm{\text{__}\ Al + 6\ NH_4ClO_4 \to \mathbf{4}\ Al_2O_3 + 2\ AlCl_3 + 3\ N_2 + 12\ H_2O}.$$
Tenslotte doen we de Al-atomen; rechts zijn er 8 van de Al2O3 en 2 van de AlCl3, dus 10 in totaal:
$$\mathrm{\mathbf{10}\ Al + 6\ NH_4ClO_4 \to 4\ Al_2O_3 + 2\ AlCl_3 + 3\ N_2 + 12\ H_2O}.$$
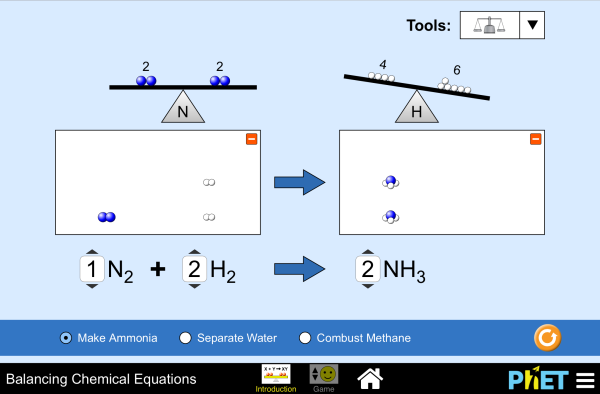
In deze simulatie kun je het kloppend maken van reacties oefenen: